FYPRYST Spot On für mittelgroße Hunde M (10-20 kg). Zur Vorbeugung und Behandlung von Infektionen durch Flöhe, Zecken oder Haarläuse bei Hunden.
GEBRAUCHSINFORMATION
1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH IST
TAD Pharma GmbH, Heinz-Lohmann-Straße 5,
27472 Cuxhaven, Deutschland
2. BEZEICHNUNG DES TIERARZNEIMITTELS
Fypryst® 67/134/268/402 mg Lösung zum Auftropfen für Hunde
Fipronil
3. WIRKSTOFF(E) UND SONSTIGE BESTANDTEILE
Jede Einzeldosis (Pipette) enthält:
| Einzeldosis |
Wirkstoff |
Stärke |
Sonstiger Bestandteil
Butylhydro-xyanisol (E320) |
Sonstiger Bestandteil
Butylhydro-xyanisol (E321) |
|
Fypryst
67 mg
|
Fipronil |
67 mg |
0,134 mg |
0,067 mg |
Fypryst
134 mg |
Fipronil |
134 mg |
0,27 mg |
0,13 mg |
Fypryst
268 mg |
Fipronil |
268 mg |
0,54 mg |
0,27 mg |
Fypryst
402 mg |
Fipronil |
402 mg |
0,80 mg |
0,40 mg |
Hellgelbe bis gelbe, klare Lösung.
4. ANWENDUNGSGEBIET(E)
Zur Behandlung eines Floh- (Ctenocephalides spp.) und Zeckenbefalls (Dermacentor reticulatus).
Zur Behandlung von Haarlingen (Trichodectes canis) bei Hunden. Die meisten Haarlinge werden innerhalb von 2 Tagen abgetötet. Die insektizide Wirkung gegen einen erneuten Befall mit adulten Flöhen bleibt bis zu 8 Wochen erhalten.
Das Tierarzneimittel hat eine persistierende akarizide Wirkung von bis zu 3 Wochen gegen Ixodes ricinus und von bis zu 4 Wochen gegen Rhipicephalus sanguineus und Dermacentor reticulatus. Sind bereits zum Zeitpunkt der Applikation des Tierarzneimittels bestimmte Arten von Zecken (Ixodes ricinus, Rhipicephalus sanguineus) am Tier vorhanden, werden möglicherweise nicht alle Zecken innerhalb der ersten 48 Stunden abgetötet.
Das Tierarzneimittel kann als Teil eines Behandlungsplans zur Kontrolle der Flohallergiedermatitis (FAD) verwendet werden, sofern diese zuvor durch einen Tierarzt diagnostiziert wurde.
5. GEGENANZEIGEN
Nicht anwenden bei Welpen, die jünger als 2 Monate sind und/oder weniger als 2 kg wiegen, da hierfür keine Untersuchungen vorliegen.
Nicht anwenden bei erkrankten (z. B. systemische Krankheiten, Fieber…) oder rekonvaleszenten Tieren.
Nicht bei Kaninchen anwenden, da Nebenwirkungen mit Todesfolge auftreten können.
Dieses Tierarzneimittel ist speziell für Hunde entwickelt worden. Nicht bei Katzen anwenden, da dies zu einer Überdosierung führen kann.
Nicht anwenden bei bekannter Überempfindlichkeit gegenüber dem Wirkstoff, Dimethylsulfoxid oder einem der sonstigen Bestandteile.
6. NEBENWIRKUNGEN
Wenn das Tier die Lösung ableckt, kann für kurze Zeit vermehrter Speichelfluss auftreten.
Zu den äußerst seltenen Nebenwirkungen nach der Anwendung gehören vorübergehende Hautreaktionen an der Applikationsstelle (Schuppen, lokaler Haarausfall, Juckreiz, Hautrötung) und allgemeiner Juckreiz oder Haarausfall. In Ausnahmefällen wurden nach der Anwendung vermehrter Speichelfluss, reversible neurologische Symptome (Hyperästhesie, Depression, nervöse Symptome), Erbrechen oder respiratorische Symptome beobachtet.
Falls Sie Nebenwirkungen, insbesondere solche, die nicht in der Packungsbeilage aufgeführt sind, bei Ihrem Tier feststellen, teilen Sie diese Ihrem Tierarzt oder Apotheker mit.
7. ZIELTIERART(EN)
Hund
8. DOSIERUNG FÜR JEDE TIERART, ART UND DAUER DER ANWENDUNG
Verabreichung und Dosierung:
Nur zur äußerlichen Anwendung.
Topische Anwendung auf der Haut entsprechend dem Körpergewicht, wie folgt:
| Hunde |
Anzahl der Pipetten |
Pipettenvolumen |
Potenz |
| über 2 kg und bis zu 10 kg |
1 Pipette |
0,67 ml |
67 mg |
| über 10 kg und bis zu 20 kg |
1 Pipette |
1,34 ml |
134 mg |
| über 20 kg und bis zu 40 kg |
1 Pipette |
2,68 ml |
268 mg |
| über 40 kg und bis zu 60 kg |
1 Pipette |
4,02 ml |
402 mg |
| über 60 kg |
1 Pipette
+
entsprechend kleinere Pipette |
4,02 ml
+
entsprechende Kombination |
402 mg
+
entsprechende Kombination
|
Art der Anwendung:
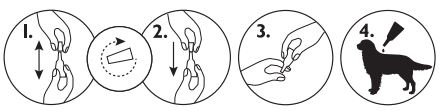
- Die Pipette aus der Folienverpackung lösen. Die Pipette aufrecht halten, die Verschlusskappe drehen und abziehen.
- Die Kappe umdrehen und mit dem anderen Ende wieder auf die Pipette setzen. Die Kappe drücken und drehen, bis der Verschluss bricht. Dann die Kappe von der Pipette entfernen.
- Das Fell des Tieres zwischen den Schulterblättern scheiteln, so dass die Haut sichtbar wird.
- Setzen Sie die Pipettenspitze auf die Haut und drücken Sie die Pipette mehrmals, um den Inhalt möglichst an 1 oder 2 Stellen direkt auf der Haut zu entleeren.
9. HINWEISE FÜR DIE RICHTIGE ANWENDUNG
Es ist wichtig sicherzustellen, dass das Tierarzneimittel an einer Stelle aufgebracht wird, wo das Tier es nicht ablecken kann und auch, dass die Tiere sich nach der Behandlung nicht gegenseitig ablecken können.
Das Fell sollte gescheitelt und das Tierarzneimittel direkt auf die Haut aufgetragen werden. Zeitweilige Veränderungen des Haarkleides (verklumptes, schmieriges Fell und/oder Ablagerungen im Fell) können an der Applikationsstelle auftreten.
Zur optimalen Kontrolle eines Floh- und/oder Zeckenbefalls sollte der Behandlungsplan die örtlichen epidemiologischen Gegebenheiten berücksichtigen.
Wegen fehlender Sicherheitsstudien sollte ein Behandlungsintervall von 4 Wochen nicht unterschritten werden.
10. WARTEZEIT
Nicht zutreffend.
11. BESONDERE LAGERUNGSHINWEISE
Arzneimittel unzugänglich für Kinder aufbewahren.
Im Originalbehältnis aufbewahren, um den Inhalt vor Licht und Feuchtigkeit zu schützen. Bis zum Gebrauch nicht aus der Folienverpackung nehmen.
Das Tierarzneimittel sollte vor der Verabreichung für ca. eine Stunde bei Raumtemperatur (über 14°C) aufbewahrt werden.
Sie dürfen das Tierarzneimittel nach dem auf dem Behältnis und äußerer Umhüllung angegebenen Verfalldatum nicht mehr anwenden.
Die Tiere müssen vor der Behandlung genau gewogen werden.
Den Kontakt mit den Augen des Tieres vermeiden. Wenn das Tierarzneimittel versehentlich in die Augen gelangt, müssen diese sofort und gründlich mit Wasser gespült werden.
Es ist wichtig sicherzustellen, dass das Tierarzneimittel an einer Stelle aufgebracht wird, wo das Tier es nicht ablecken kann und auch, dass die Tiere sich nach der Behandlung nicht gegenseitig ablecken können.
Das Tierarzneimittel nicht auf Wunden oder Hautläsionen auftragen.
Laboruntersuchungen mit Fipronil ergaben keine Hinweise auf teratogene oder embryotoxische Wirkungen. Es wurden keine Studien mit diesem Tierarzneimittel bei tragenden und säugenden Hündinnen durchgeführt.
Daher sollte eine Anwendung während der Trächtigkeit und Laktation nur nach entsprechender Nutzen-RisikoBewertung durch den behandelnden Tierarzt erfolgen.
In Verträglichkeitsstudien an Welpen im Alter von 8 Wochen, heranwachsenden Hunden und Hunden mit einem Gewicht von ungefähr 2 kg wurden nach einmaliger Anwendung der fünffachen empfohlenen Dosis keine Nebenwirkungen beobachtet. Das Risiko von Nebenwirkungen (siehe Abschnitt 6) kann jedoch im Falle einer Überdosierung steigen, daher sollten die Tiere immer mit der korrekten Pipettengröße entsprechend dem Körpergewicht behandelt werden.
Fipronil darf nicht in Gewässer gelangen, da es eine Gefahr für Wasserorganismen darstellen kann. Hunde dürfen für 2 Tage nach der Behandlung nicht in offenen Gewässern baden.
Vorsichtsmaßnahmen für den Anwender
Dieses Tierarzneimittel kann Reizungen der Schleimhaut und der Augen verursachen. Daher sollte der Kontakt mit Mund oder Augen vermieden werden.
Wenn das Tierarzneimittel versehentlich in die Augen gelangt, müssen diese sofort und gründlich mit Wasser gespült werden. Wenn die Augenreizung bestehen bleibt, ist unverzüglich ein Arzt zu Rate zu ziehen und die Packungsbeilage oder das Etikett vorzuzeigen.
Während der Anwendung nicht essen, trinken oder rauchen.
Den Kontakt mit der Haut vermeiden. Wenn das Tierarzneimittel versehentlich auf die Haut gelangt, muss diese sofort mit Wasser und Seife gewaschen werden.
Nach der Anwendung Hände waschen.
Personen mit bekannter Überempfindlichkeit gegenüber Fipronil oder Dimethylsulfoxid oder einem der übrigen Bestandteile sollten den Kontakt mit dem Tierarzneimittel vermeiden.
Den direkten Kontakt mit behandelten Tieren vermeiden, solange die Applikationsstelle noch feucht ist. Kinder sind während dieser Zeit vom behandelten Tier fern zu halten. Es wird daher empfohlen, Tiere nicht während des Tages, sondern am frühen Abend zu behandeln.
Frisch behandelte Tiere sollten nicht bei den Besitzern, insbesondere Kindern schlafen.
Pipetten in der Originalverpackung aufbewahren und gebrauchte Pipetten sofort entsorgen.
13. BESONDERE VORSICHTSMAßNAHMEN FÜR DIE ENTSORGUNG VON NICHT VERWENDETEM ARZNEIMITTEL ODER VON ABFALLMATERIALIEN, SOFERN ERFORDERLICH
Nicht aufgebrauchte Tierarzneimittel sind vorzugsweise bei Schadstoffsammelstellen abzugeben. Bei gemeinsamer Entsorgung mit dem Hausmüll ist sicherzustellen, dass kein missbräuchlicher Zugriff auf diese Abfälle erfolgen kann. Tierarzneimittel dürfen nicht mit dem Abwasser bzw. über die Kanalisation entsorgt werden.
Fipronil darf nicht in Gewässer gelangen, da es eine Gefahr für Wasserorganismen darstellen kann.
14. GENEHMIGUNGSDATUM DER PACKUNGSBEILAGE
Februar 2015
15. WEITERE ANGABEN
Weiße Pipette aus Polypropylen, mit einer Verschlusskappe aus Polyethylen oder Polyoxymethylen.
Jede Pipette ist in eine Dreifach-Umhüllung aus LD-Polyethylen/Terephthalat/Aluminium abgepackt.
Packungen mit 1, 3, 6, 10, 20 oder 30 Pipetten.
Es werden möglicherweise nicht alle Packungsgrößen in Verkehr gebracht.
Falls weitere Informationen über das Tierarzneimittel gewünscht werden, setzen Sie sich bitte mit dem örtlichen Vertreter des Zulassungsinhabers in Verbindung.